回应模式 - No.67966375
No.67966375 - 科学
讲讲尼帕病毒无名氏No.67966375 只看PO
2026-01-29(四)17:46:58 ID:bm3TlAS 回应
( ゚∀。)7
这几天看到相关的谣言传言不少,所以感觉有必要单独讲一讲,用的相关资料主要是世卫组织的资料
无标题中科院武汉病毒研究所No.68024450
2026-02-06(五)17:47:32 ID: bm3TlAS (PO主)
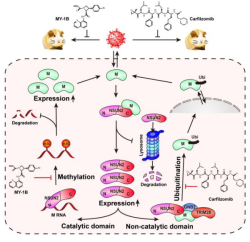
【研究发现宿主RNA表观修饰酶NSUN2调控尼帕病毒复制机制】
尼帕病毒是一种高度致病的人畜共患病毒,可引发严重的呼吸道疾病和致死性脑炎。然而,目前针对尼帕病毒尚无获批的特异性抗病毒药物或疫苗,其复制与致病机制仍不明晰。
近日,中国科学院武汉病毒研究所研究团队,发现宿主RNA表观修饰酶NSUN2被纳入病毒复制调控网络,成为连接RNA甲基化与蛋白翻译后调控的关键枢纽。
研究发现,感染发生后,病毒基质蛋白M与NSUN2直接相互作用,抑制其经由蛋白酶体途径的降解,明显提高细胞内NSUN2的稳定性和丰度,为后续病毒RNA修饰和蛋白调控过程奠定了分子基础。在RNA层面,NSUN2通过其催化结构域,在尼帕病毒RNA上催化5-甲基胞嘧啶(m5C)修饰。研究显示,病毒基因组RNA及多种病毒mRNA均存在明显m5C修饰,其中编码M蛋白的mRNA是重要靶标之一。m5C修饰明显增强病毒RNA的稳定性,使其在细胞内得以持续存在并高效翻译,从而维持关键病毒蛋白的充足表达。当NSUN2的甲基转移酶活性受到抑制,或关键修饰位点被破坏时,病毒RNA更易发生降解,病毒复制能力随之下降。
除RNA修饰功能外,NSUN2还通过其非催化结构域,参与病毒蛋白的翻译后调控。作为分子支架,NSUN2可招募泛素接头蛋白GNB2,并进一步促进E3泛素连接酶TRIM28与病毒M蛋白形成复合物,驱动其发生特定类型的泛素化修饰。这一泛素化过程对M蛋白的细胞内转运和功能发挥具有重要影响,从而在蛋白层面进一步支持病毒复制。由此,NSUN2通过催化与非催化结构域的分工协作,在RNA甲基化与蛋白泛素化两个层面,形成一套相互衔接的调控机制:一方面稳定病毒RNA,保障关键蛋白的持续表达;另一方面调控核心病毒蛋白的功能状态,共同推动尼帕病毒在宿主细胞内高效复制。
基于这一机制框架,靶向宿主依赖性通路的抗病毒潜力也得到了验证。研究证实,蛋白酶体抑制剂carfilzomib以及抑制m5C修饰的小分子MY-1B,均能有效抑制尼帕病毒复制,并在动物模型中降低病毒载量和组织损伤。联合干预两条通路时,可同时削弱病毒RNA稳定性和蛋白功能调控,产生更为明显的抗病毒效果。
该研究揭示了尼帕病毒如何通过劫持单一宿主因子,在RNA表观修饰与蛋白泛素化两个层面,协同调控病毒复制的分子机制。这一发现深化了学界对高致病性RNA病毒宿主依赖性的理解,也为发展宿主导向型、联合靶向的抗病毒策略提供了新思路和理论依据。
相关研究成果发表在Protein&Cell上。
无标题无名氏No.68024462
2026-02-06(五)17:48:21 ID: bm3TlAS (PO主)
近期,中国科学院武汉病毒研究所肖庚富/张磊砢研究员团队、单超研究员团队联合上海药物研究所、旺山旺水生物医药股份有限公司胡天文博士在国际期刊Emerging Microbes & Infections上发表了题为“The oral nucleoside drug VV116 is a promising candidate for treating Nipah virus infection”的重要研究成果,证实口服核苷类药物VV116对尼帕病毒具有显著的抗病毒活性,为这一高致死性新发传染病的防治带来新希望。